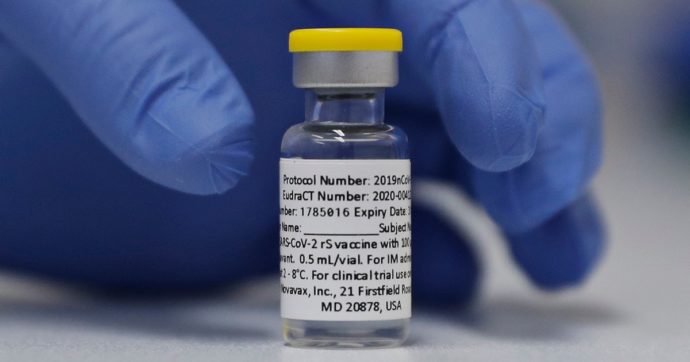
Uno dei prossimi vaccini in dirittura d’arrivo è lo statunitense NVX-CoV2373 a base di proteine ingegnerizzate della biotech statunitense Novavax con cui l’Unione europea ha una trattativa in corso da diverse settimane. Il composto è sottoposto alla rolling review da parte dell’Agenzia europea del farmaco (Ema). “Prevediamo di presentare l’approvazione regolamentare prima nel Regno Unito con la Mhra (Medicines and Healthcare products Regulatory Agency, ndr) nel secondo trimestre. Abbiamo già iniziato il processo di presentazione con Ema e diverse altre agenzie con dati non clinici. Una volta che avremo completato il processo di presentazione – spiega al fattoquotidiano.it ha John Trizzino, vicepresidente esecutivo, Chief Commercial e Business Novavax – l’Ema completerà la sua revisione, che determinerà la tempistica definitiva”.
DOSI, TEMPI E ACCORDI – Sulla questione contrattuale ancora ci sono delle incognite “i nostri negoziati con l’Europa sono in corso, i dettagli sulle quantità e sui tempi non sono ancora disponibili”. Ancora non c’è una data definitiva, e alla domanda se sia ipotizzabile che le dosi del vaccino Novavax possano arrivare in Italia entro la seconda metà di maggio, il vicepresidente ha risposto che “la disponibilità finale dipenderà da quando l’Ema completerà la sua revisione. Attualmente stiamo discutendo con la Commissione europea i termini di un accordo di acquisto”. Mentre, sul versante della capacità produttiva le idee sono chiare ”nel complesso, ci aspettiamo una capacità di produzione di circa 150 milioni di dosi al mese entro il terzo trimestre, ciò include la capacità proveniente dal nostro partner, il Serum Institute of India”. In questa partita è entrato anche il governo del Regno Unito, che si è assicurato 60 milioni di dosi del vaccino in base a un accordo di acquisto anticipato con Novavax.
Il componente dell’antigene proteico di NVX-CoV2373 è prodotto anche nel nord-est dell’Inghilterra dal partner di produzione di Novavax, Fujifilm Diosynth Biotechnologies, nel sito di Billingham, Stockton-on-Tees. La “Fill and finish”, ovvero la fase di completamento della produzione del vaccino, sarà coadiuvata da Gsk (nel sito di Barnard Castle), con la quale Novavax ha raggiunto un accordo triangolato insieme alla task force del governo britannico. Infine, John Trizzino ci rivela che “Sì, abbiamo accordi con Giappone, India, Corea del Sud, Australia e Nuova Zelanda. Ci siamo anche impegnati, insieme al nostro partner Serum Institute of India, per un totale di 1,1 miliardi di dosi di vaccino per la struttura COVAX (Oms)”.
CHE TIPO DI VACCINO È? COME FUNZIONA? – “Il nostro vaccino ha diversi elementi di differenziazione e vantaggi – chiarisce il vicepresidente – usiamo un quantità molto piccola di antigene. Questo fornisce una capacità di creare un vaccino multivalente e una rapida creazione/produzione su larga scala di candidati vaccinali che potrebbero affrontare più ceppi in circolazione”, a questo va aggiunto che “nei test preclinici, è sembrato indurre un’immunità sterile”, quindi chi fa il vaccino non dovrebbe poter contagiare altre persone, questo stando ai dati attuali. Una novità è l’uso dell’adiuvante il Matrix-M™, brevettato dalla Novavax, a base di saponina che “ha dimostrato un effetto potente e ben tollerato stimolando l’ingresso delle cellule che presentano l’antigene nel sito di iniezione e migliorando l’efficacia del vaccino, e migliorando la presentazione dell’antigene nei linfonodi locali, potenziando la risposta immunitaria”.
L’adiuvante quindi “ha sia un effetto di rafforzamento immunitario che di riduzione della dose”. Il vaccino può essere spedito e conservato alle tipiche temperature di refrigerazione (2-8◦C), “questo permetterà di distribuirlo attraverso i canali di fornitura di vaccini esistenti”. Allo stato attuale il vaccino risulta “efficace contro le varianti, confermata nei trials del Regno Unito e in Sudafrica (in percentuale inferiore). L’efficacia è stata del 96,4% contro il ceppo originale del virus e dell’86,3% contro la variante inglese (B.1.1.7/501Y.V1) circolante nel Regno Unito. Nello studio di Fase 2b in Sud Africa ha dimostrato un’efficacia del 48,65% contro la variante emergente (sudafricana, ndr)”, parrebbe non destare preoccupazioni la capacità del vaccino di indurre eventi avversi, “ad oggi, il vaccino ha dimostrato un forte profilo di sicurezza, senza gravi eventi avversi”. Questi i dati provenienti dalla sperimentazione più avanzata di Fase 3 nel Regno Unito. In Uk lo studio ha arruolato più di 15.000 partecipanti di età compresa tra 18-84 anni, di cui il 27% con più di 65 anni. Gli adulti anziani sono tra i gruppi più colpiti dalla malattia e sono ad alto rischio di complicazioni da Covid 19. Nei volontari di 65 anni e più, sono stati osservati 10 casi di COVID-19, e il 90% di questi casi si è verificato nel gruppo placebo.
Articolo Precedente
CureVac, il terzo vaccino a mRna che può far svoltare l’Ue. L’azienda: “Produrremo 300 milioni di dosi nel 2021. Si conserva a 5 gradi”

Articolo Successivo
AstraZeneca e seconda dose, Abrignani (Cts): “Richiamo con vaccino diverso ha molto senso, a livello immunologico è meglio”