Vaccino Covid, Ema sulla terza dose: “Stati possono già considerare i piani preparatori ma decide chi guida campagne vaccinali”
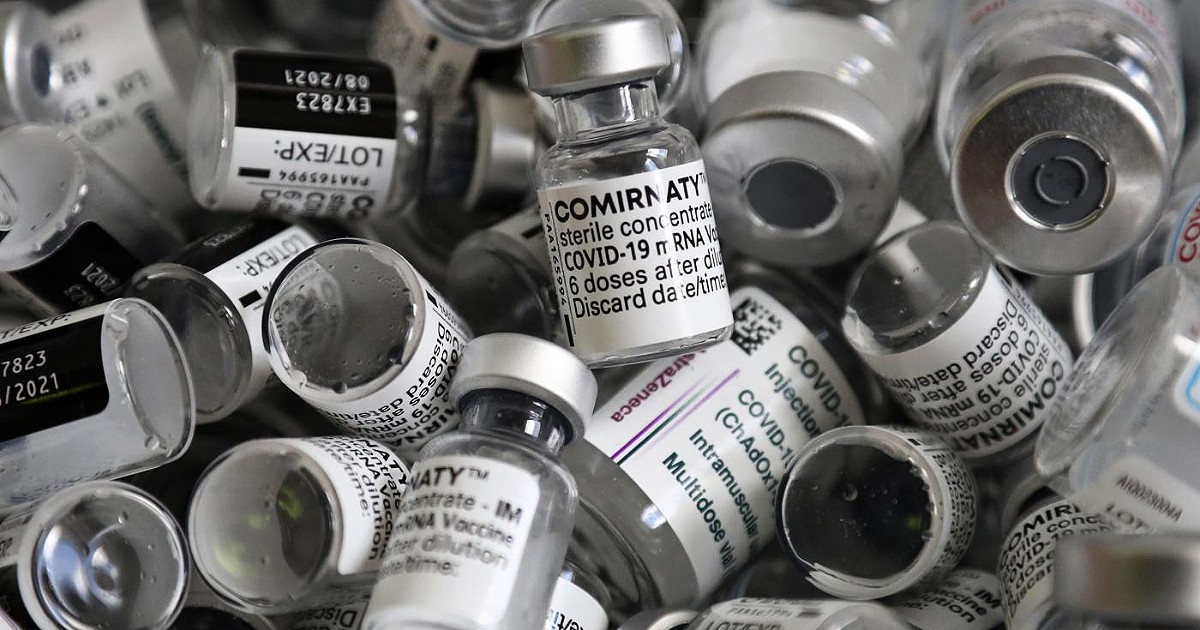
Nei giorni scorsi l'Agenzia europea del farmaco aveva informato in una nota congiunta con il Centro europeo per la prevenzione e il controllo delle malattie (Ecdc) che la terza somministrazione era necessaria per le persone immunodepresse
La terza dose di vaccino anti Covid già somministrata in alcuni paesi come Israele torna nuovamente all’attenzione della valutazione dell’Agenzia europea del farmaco. Nei giorni scorsi l’Ema aveva informato in una nota congiunta con il Centro europeo per la prevenzione e il controllo delle malattie (Ecdc) che la terza somministrazione era necessaria per le persone immunodepresse. Oggi da Amsterdam arriva una precisazione ovvero che la consulenza su come somministrare le vaccinazioni rimane prerogativa dei gruppi consultivi tecnici nazionali sull’immunizzazione (Nitag) che guidano le campagne vaccinali” anti-Covid “in ciascuno Stato membro dell’Ue”. Per questo, “mentre l’Ema valuta i dati” sul cosiddetto ‘booster’, “gli Stati membri possono già prendere in considerazione piani preparatori per la somministrazione di richiami e dosi aggiuntive”.
L’Ema oggi ha annunciato di avere “iniziato a valutare una domanda per l’uso di una dose di richiamo di Comirnaty”, il composto di Pfizer/BioNTech, “da somministrare 6 mesi dopo la seconda dose a persone di età pari o superiore a 16 anni”. L’ente regolatorio, “separatamente”, sta anche “valutando i dati della letteratura sull’uso di una terza dose aggiuntiva di un vaccino a mRna SpikeVax (il prodotto di Moderna, ndr) – in persone gravemente immunocompromesse”.
“Mentre queste valutazioni sono in corso – ricorda l’Agenzia – l’Ema e l’Ecdc, il Centro europeo per la prevenzione e il controllo delle malattie, hanno evidenziato la loro posizione attuale in una comunicazione separata” diffusa la scorsa settimana. “Sebbene Ema ed Ecdc”, come si spiegava in quella nota, “non considerino urgente la necessità di dosi di richiamo del vaccino Covid-19 nella popolazione generale, l’Ema sta valutando la domanda” del produttore di Comirnaty “per garantire che siano disponibili prove a sostegno di ulteriori dosi, se necessario”.
“Il comitato per i medicinali umani dell’Ema – si legge nella nota – effettuerà una valutazione accelerata dei dati presentati dalla società che commercializza Comirnaty, compresi i risultati di uno studio clinico in corso in cui circa 300 adulti con sistema immunitario sano hanno ricevuto una dose di richiamo circa 6 mesi dopo la seconda dose”. L’esito della valutazione, precisa l’Ema, è atteso nelle prossime settimane, a meno che non siano necessarie informazioni supplementari. Anche Moderna nei giorni scorsi ha presentato all’Ema uno studio.
Intanto la statunitense Food and Drug Administration venerdì 17 settembre si riunirà con il comitato consultivo sui vaccini e i prodotti biologici correlati per discutere la questione. Il confronto, in programma dalle 8.30 alle 15.45 locali (in Italia 11.30-21.45), riguarderà in particolare la richiesta di autorizzazione supplementare avanzata da Pfizer/BioNTech per la somministrazione di una terza dose del vaccino a mRna Comirnaty* nelle persone di età pari a 16 o maggiori. L’incontro sarà trasmesso dalla Fda sul sito e sul canale YouTube dell’ente. “L’amministrazione ha recentemente annunciato un piano per prepararsi alla somministrazione di ulteriori dosi di vaccino contro Covid-19, questo autunno – spiega Peter Marks, direttore del Center for Biologics Evaluation and Research (Cber) della Fda – e una parte fondamentale di questo piano è il completamento di una valutazione indipendente e la determinazione da parte dell’agenzia della sicurezza e dell’efficacia di queste dosi aggiuntive”.
“Il processo” per autorizzare un’eventuale dose booster, precisa Marks, “prevede che ciascun produttore di vaccini presenti all’agenzia dati relativi alla sicurezza e all’efficacia per supportare questo utilizzo. La Fda sta valutando i dati presentati da Pfizer-BioNTech” nella sua domanda e “ne discuterà con il suo comitato consultivo”. “Una revisione trasparente, approfondita e obiettiva dei dati da parte della Fda – rimarca il direttore del Cber – è fondamentale affinché la comunità medica e il pubblico continuino ad avere fiducia nella sicurezza e nell’efficacia dei vaccini Covid-19. La Fda esaminerà la richiesta” della compagnia farmaceutica statunitense e del suo partner tedesco “il più rapidamente possibile, pur continuando a farlo in modo approfondito e basato sulla scienza”.