Covid, l’Agenzia europea del farmaco dà il via libera ai vaccini adattati per Omicron
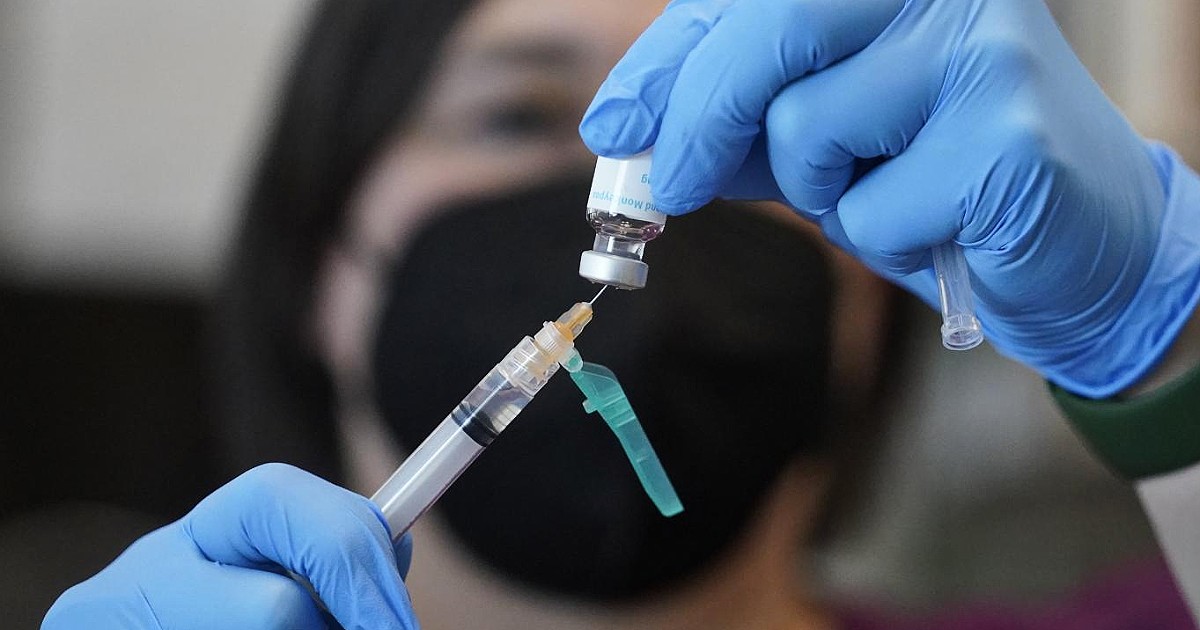
Spiega l'Ema che i due vaccini bivalenti possono innescare forti risposte immunitarie contro Omicron BA.1 e il ceppo originale SarsCov2 in persone precedentemente vaccinate. Sono in fase di revisione vaccini riguardanti le subvarianti BA.4 e BA.5, attualmente in circolazione
Il comitato per i medicinali umani dell’Agenzia europea del farmaco (Ema) ha raccomandato di autorizzare due vaccini adattati per fornire una protezione più ampia contro il Covid-19. Si tratta di Comirnaty Original/Omicron BA.1 e Spikevax Bivalent Original/Omicron BA.1, di Pfizer Biontech e Moderna. Sono destinati a persone di età pari o superiore a 12 anni che hanno ricevuto almeno la vaccinazione primaria contro Covid-19. Lo annuncia l’Ema.
Spiega l’Ema che studi hanno dimostrato che i due vaccini bivalenti possono innescare forti risposte immunitarie contro Omicron BA.1 e il ceppo originale SarsCov2 in persone precedentemente vaccinate. In particolare, sono più efficaci nell’innescare risposte immunitarie contro la subvariante BA.1 rispetto ai vaccini originali. Gli effetti collaterali osservati nei vaccini adattati sono paragonabili a quelli dei vaccini originali: tipicamente lievi e di breve durata. I due pareri del CHMP saranno ora trasmessi alla Commissione europea, che adotterà una decisione finale.
Altri vaccini adattati che incorporano diverse varianti, come le subvarianti BA.4 e BA.5 di Omicron – le varianti in circolazione – sono attualmente in fase di revisione da parte dell’Ema o saranno presto presentati e, se autorizzati, estenderanno ulteriormente l’arsenale dei vaccini disponibili. I dati clinici generati con i vaccini bivalenti originali/BA.1 raccomandati oggi supporteranno la valutazione e l’autorizzazione di ulteriori vaccini adattati. L’agenzia del farmaco spiega anche che i vaccini originali, Comirnaty e Spikevax, sono ancora efficaci nella prevenzione di malattie gravi, ospedalizzazione e decesso associati a Covid-19 e continueranno ad essere utilizzati nelle campagne di vaccinazione nell’Ue, in particolare per le vaccinazioni primarie.
Le autorità nazionali degli Stati membri dell’Ue determineranno chi dovrebbe ricevere quali vaccini e quando, tenendo conto di fattori quali i tassi di infezione e di ospedalizzazione, il rischio per le popolazioni vulnerabili, la copertura vaccinale e la disponibilità di vaccini. I vaccini adattati funzionano allo stesso modo dei vaccini originali: ciascun vaccino contiene le molecole mRna con le istruzioni sulle proteine spike del SarsCov2 originale e della subvariante BA.1 di Omicron. Lo precisa la stessa Ema.
“Attendiamo ora il via libera di Aifa, (l’Agenzia italiana del farmaco, ndr) previsto per lunedì 5 settembre, e poi potremo partire già nelle prossime settimane a somministrare il vaccino bivalente”. Ha fatto sapere il sottosegretario alla Salute Andrea Costa. “Ancora una volta la scienza e la ricerca si dimostrano asset strategici, decisivi e irrinunciabili per affrontare le grandi sfide sanitarie del futuro”, conclude Costa.